Contenido
1) Idea general
El átomo de hidrógeno (un protón \(+e\) y un electrón \(-e\)) posee niveles de energía discretos \(n=1,2,3,\ldots\). La luz puede ser absorbida si su energía coincide con la diferencia entre dos niveles permitidos y emitida cuando el electrón regresa a un estado de menor energía. El modelo de Bohr captura los valores de energía y el patrón espectral.
2) Imagen 0 — Fuerzas: electrostática y centrípeta
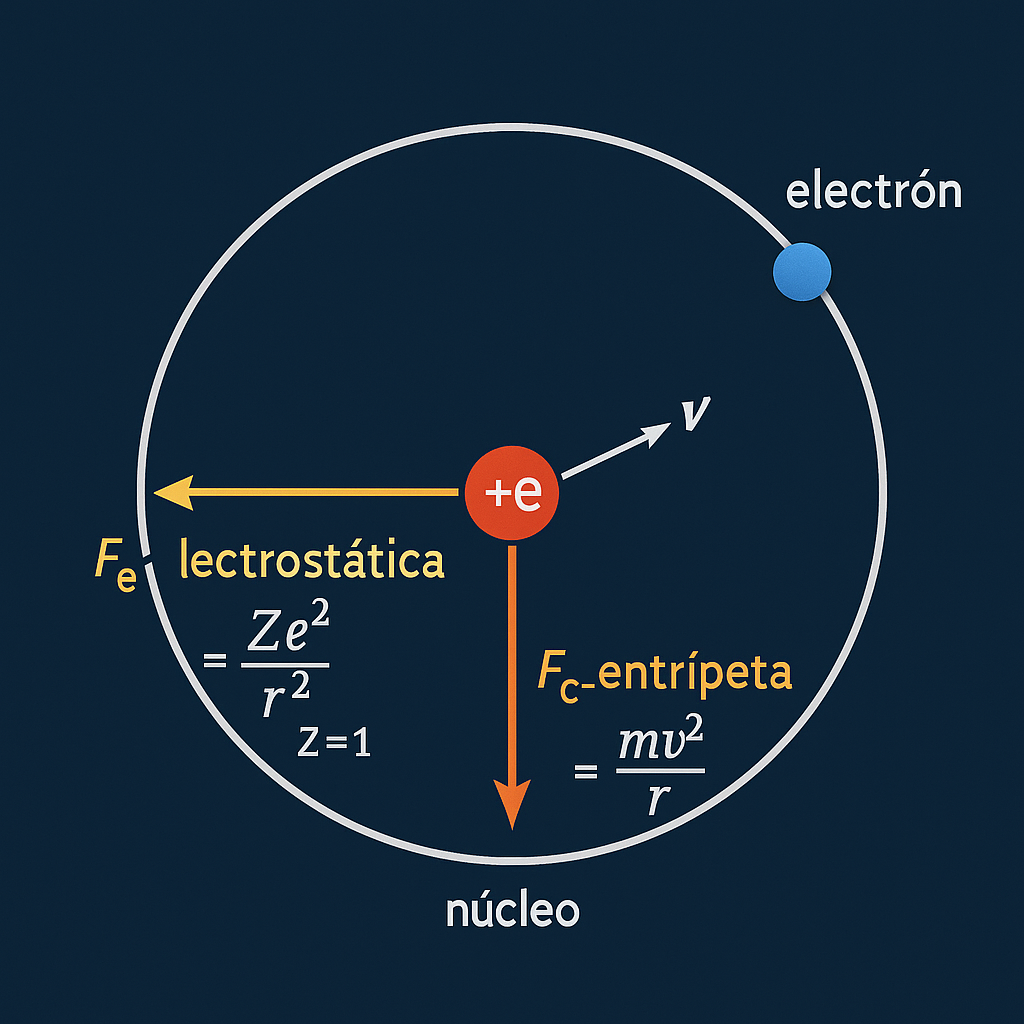
Discusión
La fuerza electrostática atrae al electrón hacia el núcleo, mientras que el movimiento curvo del electrón requiere una aceleración centrípeta. En estado estacionario del modelo de Bohr se cumple \(\frac{Z e^2}{r^2}=\frac{m v^2}{r}\), ecuación base para deducir los radios permitidos combinada con la cuantización del momento angular.
Analogía
Piensa en una piedra atada a una cuerda girando en círculo: la tensión (aquí, atracción electrostática) es la que mantiene la trayectoria. Si esa fuerza cambiara, también lo haría el radio de la órbita.
3) Imagen 1 — Niveles y series espectrales
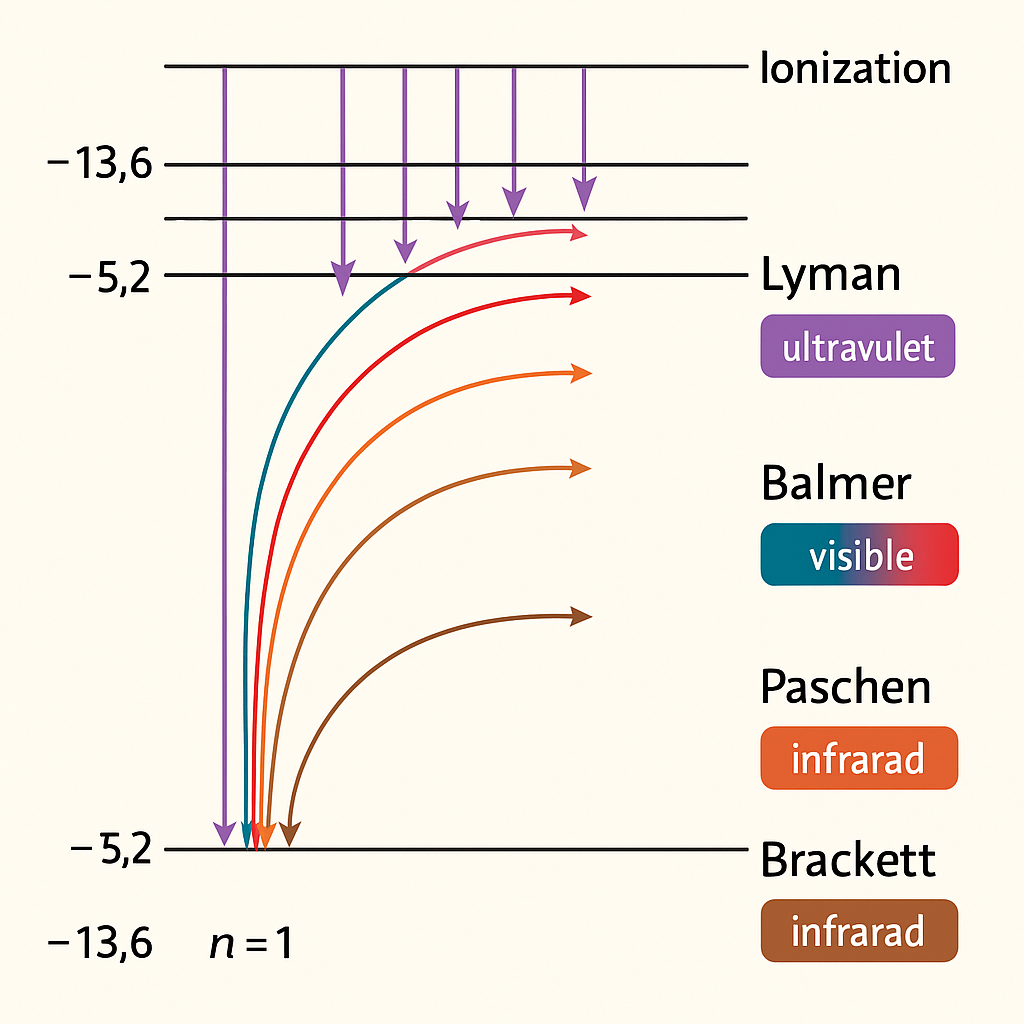
Discusión
En el átomo de hidrógeno, el electrón solo puede ocupar ciertos niveles de energía cuantizados, numerados por \(n = 1, 2, 3, \dots\). Estos niveles no son continuos como una rampa, sino discretos, como los escalones de una escalera: el electrón no puede “existir” entre ellos.
Cuando el electrón salta hacia abajo desde un nivel superior \(n_i\) a uno inferior \(n_f\), emite un fotón cuya energía corresponde a la diferencia:
De forma inversa, si un fotón con energía exactamente igual a \(\Delta E\) incide sobre el átomo, puede ser absorbido y el electrón sube de nivel. Esto explica las líneas oscuras (absorción) o brillantes (emisión) en los espectros.
Cada grupo de transiciones que termina en un mismo nivel final forma una serie espectral:
- Lyman: \(n_f = 1\) → radiación ultravioleta.
- Balmer: \(n_f = 2\) → visible (rojo a violeta).
- Paschen: \(n_f = 3\) → infrarrojo cercano.
Analogía
Imagina que estás en un edificio con elevadores “inteligentes”. Cada piso es un nivel cuántico y el elevador solo se mueve si insertas exactamente la cantidad de energía requerida. Si pones menos “monedas” (energía del fotón), el elevador no se mueve; si pones más de la cuenta, te lleva a un piso todavía más alto.
Otra forma: resortes calibrados entre pisos. Cada resorte solo “salta” cuando lo cargas con el peso exacto (energía del fotón). Con poca carga no se activa; con exceso, te impulsa a un piso mayor e incluso, si es suficiente, te arroja fuera del edificio (ionización).
4) Derivaciones clave (paso a paso)
a) Equilibrio radial
b) Cuantización del momento angular
c) Radio permitido \(r_n\) en función de \(n\hbar\)
Con \(v_n=\dfrac{n\hbar}{m r_n}\) y el equilibrio radial:
d) Velocidad lineal, angular y frecuencia
5) Versión SI y constantes
Con \(4\pi\varepsilon_0\), la constante de estructura fina \(\alpha=\dfrac{e^2}{4\pi\varepsilon_0\hbar c}\) y el radio de Bohr \(a_0=\dfrac{4\pi\varepsilon_0\hbar^2}{m e^2}\):
- \(\alpha \approx 1/137.036\)
- \(a_0 \approx 5.2918\times10^{-11}\ \mathrm{m}\)
- \(E_1 = -13.6\ \mathrm{eV}\)
6) Imagen 2 — Bohr vs. Cuántico
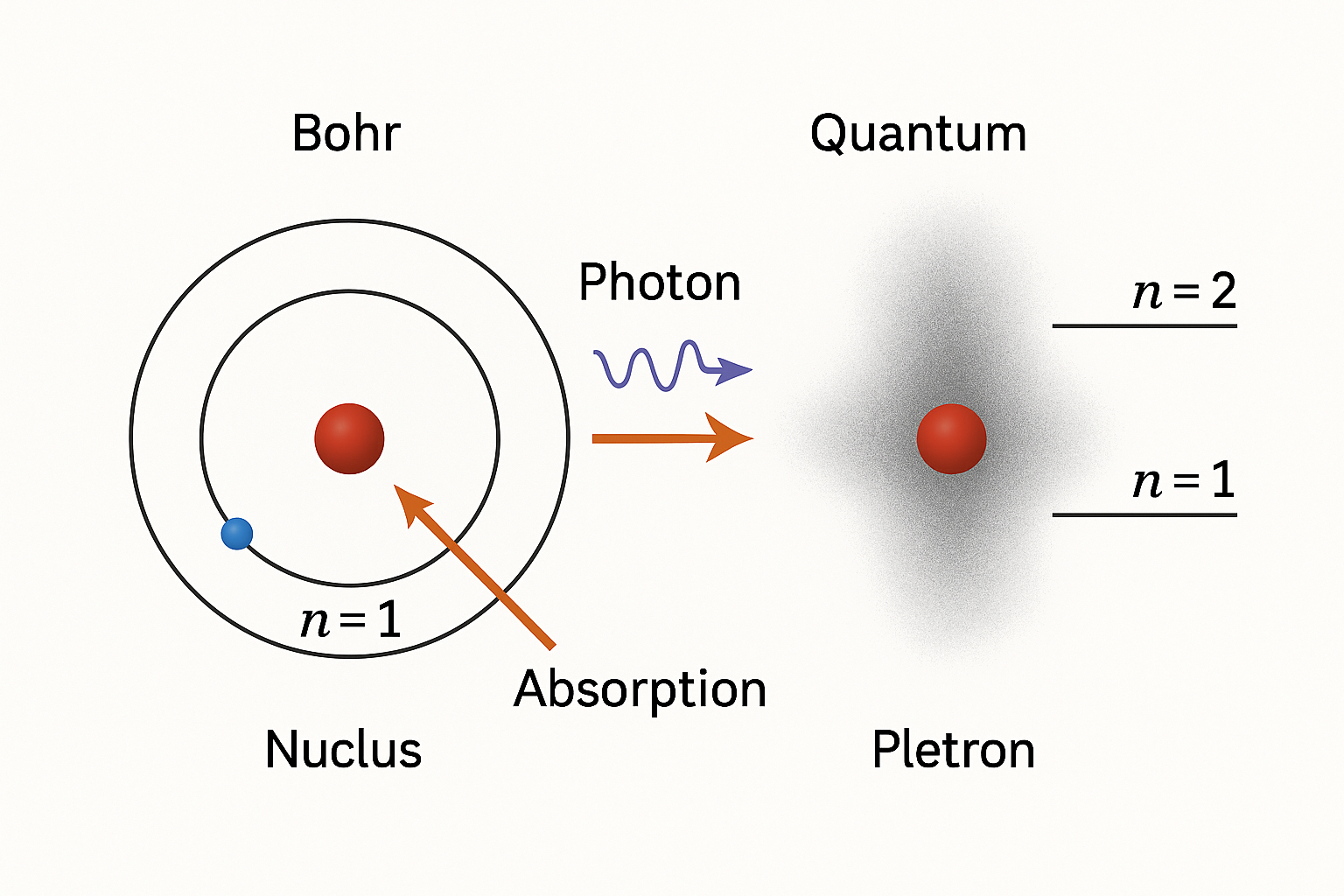
Discusión
Bohr reproduce el espectro del hidrógeno, pero la imagen orbital clásica se reemplaza por funciones de onda. La cuantización surge de condiciones de contorno de \(\psi\), no de órbitas rígidas.
Analogía
En Bohr, el electrón es como un tren en vías circulares; en cuántica, es como una niebla densa con patrones estables. Las vías (niveles) siguen existiendo, pero el “vehículo” ya no es puntual: es una distribución.
7) Valores numéricos para hidrógeno
Nivel fundamental
- \(r_1 \approx a_0 \approx 5.29\times10^{-11}\ \mathrm{m}\)
- \(v_1 \approx \alpha c \approx 2.19\times10^6\ \mathrm{m/s}\)
- \(\omega_1 \approx 4.14\times10^{16}\ \mathrm{rad/s}\)
- \(E_1=-13.6\ \mathrm{eV}\)
Transición \(n=2\to n=1\)
Línea Lyman-\(\alpha\): \(\Delta E=10.2\ \mathrm{eV}\), \(\lambda\approx 121.6\ \mathrm{nm}\) (UV).
Las transiciones hacia \(n=2\) forman la serie de Balmer (visible, 400–700 nm).
8) Preguntas frecuentes
1) ¿Por qué Bohr acierta en energías pero falla en momento dipolar y estructura fina?
Bohr impone \(L=n\hbar\) ad hoc y asume órbitas circulares. La teoría de Dirac (relativista) y el tratamiento de momento angular total \( \mathbf{J}=\mathbf{L}+\mathbf{S} \) explican la estructura fina y el desdoblamiento por espín y correcciones relativistas que Bohr no contempla.
2) ¿Cómo se deriva \(\alpha\) (estructura fina) de constantes fundamentales?
\(\displaystyle \alpha=\frac{e^2}{4\pi\varepsilon_0\hbar c}\). Es adimensional y mide la intensidad de la interacción electromagnética; en H fija \(v_1\approx \alpha c\) y escalas de energía (\(\sim \alpha^2 mc^2\)).
3) ¿Cómo se conecta Bohr con Schrödinger?
Resolviendo la ecuación de Schrödinger para el potencial Coulombiano se obtienen energías \(E_n\propto -1/n^2\), idénticas a Bohr. La cuantización emerge de las condiciones de normalización de \(\psi\), no de órbitas. Los números cuánticos \(n,\ell,m\) reemplazan la órbita clásica.
4) ¿Qué limitaciones aparecen en campos externos (Stark/Zeeman)?
Bohr no predice el desdoblamiento de niveles por campos eléctrico (Stark) o magnético (Zeeman). La teoría cuántica con perturbaciones (y espín) sí reproduce desplazamientos lineales y cuadráticos.
5) ¿Por qué el electrón no “irradiaría” continuamente al girar?
En electromagnetismo clásico sí lo haría. En Bohr, los estados estacionarios no irradian por postulado. En cuántica, el estado ligado es una solución estacionaria de Schrödinger: la densidad \(|\psi|^2\) es estática y no hay radiación salvo en transiciones discretas.
6) ¿Cómo cambian las fórmulas para iones hidrogenoides (Z>1)?
Sustituye \(Z\): \(r_n=\dfrac{n^2 a_0}{Z}\), \(v_n=\dfrac{Z\alpha c}{n}\), \(E_n=-\dfrac{13.6\,Z^2}{n^2}\ \mathrm{eV}\). Las frecuencias de transición escalan con \(Z^2\).
7) ¿De dónde sale \(\omega_n=\dfrac{m Z^2 e^4}{n^3\hbar^3}\)?
De \( \omega_n=\dfrac{v_n}{r_n} \) con \( v_n=\dfrac{Z e^2}{n\hbar}\) y \( r_n=\dfrac{n^2\hbar^2}{m Z e^2}\). Simplificando se obtiene la dependencia \( \propto Z^2/n^3 \).
8) ¿Qué corrige QED en el hidrógeno (desplazamiento de Lamb)?
Las fluctuaciones del vacío y autoenergía del electrón corrigen niveles degenerados, separando \(2S_{1/2}\) y \(2P_{1/2}\). Es una corrección más allá de Dirac que Bohr no puede anticipar.
9) ¿Cómo se conecta el espectro con reglas de selección?
Las probabilidades de transición dependen de elementos de matriz del operador dipolar eléctrico. Reglas de selección: \(\Delta \ell=\pm 1\), \(\Delta m=0,\pm 1\). Bohr ignora intensidades; la cuántica las cuantifica.
10) ¿En qué régimen fallan más las órbitas de Bohr?
En \(Z\) grande (efectos relativistas), acoplamiento espín-órbita, campos intensos, sistemas multielectrón (pantallas electrónicas, correlación) y en propiedades angulares finas (momentos dipolares, hiperfina).
9) Recomendación final
Tarea sugerida: vuelve a leer esta página y copia a mano en tu libreta todo: Añade una analogía propia a cada paso. La escritura activa consolida la memoria a largo plazo.
↺ Volver al inicio